von kaka » 28.03. 2014 13:02
Die praktisch wortgleich in einem anderen Forum gestellte Frage habe ich gestern dort so beantwortet :
ka hat geschrieben:Alex33 hat geschrieben:
Jetzt ist das Problem, dass sich bei der Gleichung alle Einheiten rauskürzen (G in J/mol, R in J/mol*K und T in K), meine Betreuerin aber ganz richtig angemerkt hat, dass K hier ne Einheit braucht lauf MWG (mol/l).
Der Betreuerin scheint nicht bewusst zu sein , dass verschiedene Gleichgewichtskonstanten in Gebrauch sind. Die sich aus
 \ = \ \Delta_rG_0(T,p) \ + \ RT \ ln \ Q_a)
 \ = \ 0 \ \ <=> \ \ Q_a \ = \ K_a \ <=>\ \Delta_rG_0(T,p) \ = \ - RT \ ln \ K_a)
ist auf dimensionslose Aktivitäten bezogen und darf nicht mit der auf Stoffmengenkonzentrationen bezogenen Gleichgewichtskonstanten Kc in einen Topf geworfen werden .
Im Übrigen : In den Werten für Aktivitäten ist im Gegensatz zu Stoffmengenkonzentrationen berücksichtigt, dass die Reaktivität eines Teilchens durch Bindungen an Teilchen des umgebenden Mediums verändert wird und die Stärke dieser Bindung auch mit dem Grad "Verdünnung" variiert. So "spürt" z.B. ein Ion in einer sehr hoch verdünnten , wässrigen Lösung praktisch nur die Wechselwirkung mit den unmittelbar umgebenden Wassermolekülen, die Wechselwirkung mit anderen Ionen, die bei einer hochverdünnten Lösung in der Regel sehr viel weiter entfernt sind, aber so gut wie nicht.
Wenn man also Aktivitäten in Konzentrationen umrechnen will, dann benötigt man u.a. einen Korrekturfaktor, den man als "Aktivitätskoeffizienten" bezeichnet. Der aber, wie das Beispiel von Ionen zeigt , nicht etwa konstant ist, sondern ( natürlich ! ) mit der Zusammensetzung des Mediums variiert.
Standardzustand eines Stoffes bedeutet also nicht nur p = 1,013 bar und T = 298,14 Kelvin, sondern auch eine Aktivität a(X) = 1.
Im Übrigen : Die SI - Einheit der freien Enthalpie G ist das "Joule". Die freie Reaktionsenthalpie hat die SI - Einheit "Joule/mol". Divigiert man die freie Enthalpie einer Stoffmenge durch eben diese Stoffmenge, so bezeichnet man den Quotienten als molare freie Enthalpie Gm Denn bei der freien Reaktionsenthalpie
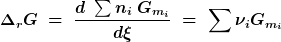
gibt die Umsatzvariable "ksi" die Zahl der Formelumsätze gemäß der jeweils zugehörigen Reaktionsgleichung in "mol Formelumsätze" an.
Zur Normierung der Aktivitäten und deren Umrechnen in Konzentrationen und Partialdrucke weitere Details auf Nachfrage.
Die praktisch wortgleich in einem anderen Forum gestellte Frage habe ich gestern dort so beantwortet :
[quote="ka"][quote="Alex33"]
Jetzt ist das Problem, dass sich bei der Gleichung alle Einheiten rauskürzen (G in J/mol, R in J/mol*K und T in K), meine Betreuerin aber ganz richtig angemerkt hat, dass K hier ne Einheit braucht lauf MWG (mol/l).[/quote]
Der Betreuerin scheint nicht bewusst zu sein , dass verschiedene Gleichgewichtskonstanten in Gebrauch sind. Die sich aus
[math]\Delta_rG_0(T.p) \ = \ \Delta_rG_0(T,p) \ + \ RT \ ln \ Q_a[/math]
[math]Gleichgewicht :\Delta_rG_0(T,p) \ = \ 0 \ \ <=> \ \ Q_a \ = \ K_a \ <=>\ \Delta_rG_0(T,p) \ = \ - RT \ ln \ K_a[/math]
ist auf dimensionslose Aktivitäten bezogen und darf nicht mit der auf Stoffmengenkonzentrationen bezogenen Gleichgewichtskonstanten Kc in einen Topf geworfen werden .
Im Übrigen : In den Werten für Aktivitäten ist im Gegensatz zu Stoffmengenkonzentrationen berücksichtigt, dass die Reaktivität eines Teilchens durch Bindungen an Teilchen des umgebenden Mediums verändert wird und die Stärke dieser Bindung auch mit dem Grad "Verdünnung" variiert. So "spürt" z.B. ein Ion in einer sehr hoch verdünnten , wässrigen Lösung praktisch nur die Wechselwirkung mit den unmittelbar umgebenden Wassermolekülen, die Wechselwirkung mit anderen Ionen, die bei einer hochverdünnten Lösung in der Regel sehr viel weiter entfernt sind, aber so gut wie nicht.
Wenn man also Aktivitäten in Konzentrationen umrechnen will, dann benötigt man u.a. einen Korrekturfaktor, den man als "Aktivitätskoeffizienten" bezeichnet. Der aber, wie das Beispiel von Ionen zeigt , nicht etwa konstant ist, sondern ( natürlich ! ) mit der Zusammensetzung des Mediums variiert.
Standardzustand eines Stoffes bedeutet also nicht nur p = 1,013 bar und T = 298,14 Kelvin, sondern auch eine Aktivität a(X) = 1.
[/quote]
Im Übrigen : Die SI - Einheit der freien Enthalpie G ist das "Joule". Die freie Reaktionsenthalpie hat die SI - Einheit "Joule/mol". Divigiert man die freie Enthalpie einer Stoffmenge durch eben diese Stoffmenge, so bezeichnet man den Quotienten als molare freie Enthalpie Gm Denn bei der freien Reaktionsenthalpie
[math]\Delta_rG \ = \ \frac {d \ \sum n_i \ G_{m_i}}{d \xi} \ = \ \sum \nu_i G_{m_i}[/math]
gibt die Umsatzvariable "ksi" die Zahl der Formelumsätze gemäß der jeweils zugehörigen Reaktionsgleichung in "mol Formelumsätze" an.
Zur Normierung der Aktivitäten und deren Umrechnen in Konzentrationen und Partialdrucke weitere Details auf Nachfrage.