Verfasst: 21.10. 2007 14:16
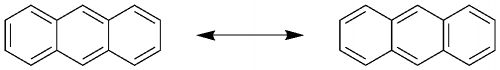
@topip: Wie kommst du auf dein Ausgangsstoff aus dem Anthracen-Teil? - Weiss ja nicht, aber sieht mir etwas seltsam aus und ich bekomme keine solche Resonanzstruktur hin?!
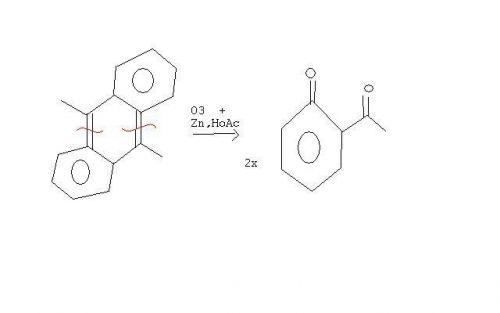
@vogelmann Tja, ob das Naphtalen-Derivat auch noch ozonolysiert würde, weiss ich natürlich auch nicht, müsste das Experiment zeigen
Weshalb ich diesen Weg beschritten bin: Wollte nicht unbedingt zwei Aromaten zerstören und fand gerade keinen besseren Weg... "Klassisch" ist ja die Ozonolyse von Phenantrenen, nicht unbedingt von Antracenen?
Grüsse
alpha
@vogelmann Tja, ob das Naphtalen-Derivat auch noch ozonolysiert würde, weiss ich natürlich auch nicht, müsste das Experiment zeigen
Weshalb ich diesen Weg beschritten bin: Wollte nicht unbedingt zwei Aromaten zerstören und fand gerade keinen besseren Weg... "Klassisch" ist ja die Ozonolyse von Phenantrenen, nicht unbedingt von Antracenen?
Grüsse
alpha