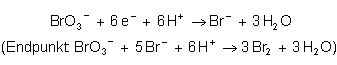Redox-Titration
Verfasst: 31.05. 2005 16:41
Ich muss demnächst Antimon bromatometrisch bestimmen. Dazu habe ich leider ein paar Fragen: Könnt ihr mir sagen wie der Stöchometrie-Faktor bei dieser Reaktion ist, also sprich das Verhältnis n(Sb)/n(BrO3)??
Mir konnt bisher keiner eine genaue Antwort geben.
Hat vielleicht jemand mit dieser Titration schon irgendwelche Erfahrungen gemacht und kann mir nützliche Tipps geben, besonders was den Farbumschlag des Indikators (Methylorange) anbedrifft?? Dieser soll nämlich etwas indifferent sein!?
Und als drittes würde es mich mal interessieren, ob man Antimon auch komplexometrisch bestimmen kann?? Falls nicht, warum eigentlich nicht?? Kann jemand sagen ob Antimon iodometrisch besser funktioniert??
Vielen Dank schonmal im vorraus...
Mir konnt bisher keiner eine genaue Antwort geben.
Hat vielleicht jemand mit dieser Titration schon irgendwelche Erfahrungen gemacht und kann mir nützliche Tipps geben, besonders was den Farbumschlag des Indikators (Methylorange) anbedrifft?? Dieser soll nämlich etwas indifferent sein!?
Und als drittes würde es mich mal interessieren, ob man Antimon auch komplexometrisch bestimmen kann?? Falls nicht, warum eigentlich nicht?? Kann jemand sagen ob Antimon iodometrisch besser funktioniert??
Vielen Dank schonmal im vorraus...