Mit der Nutzung dieses Forums (dies beinhaltet auch die Regisitrierung als Benutzer) erklärt Sie sich mit unserer Datenschutzerklärung (https://www.chemiestudent.de/impressum.php) einverstanden. Sofern Sie dieses nicht tun, dann greifen Sie bitte nicht auf unsere Seite zu. Als Forensoftware wird phpBB verwendet, welches unter der GNU general public license v2 (http://opensource.org/licenses/gpl-2.0.php) veröffentlicht wurde.
Das Verfassen eines Beitrag auf dieser Webseite erfordert keine Anmeldung und keine Angabe von persönlichen Daten. Sofern Sie sich registrieren, verweisen wir Sie auf den Abschnitt "Registrierung auf unserer Webseite" innerhalb unserer Datenschutzerklärung.
Das Verfassen eines Beitrag auf dieser Webseite erfordert keine Anmeldung und keine Angabe von persönlichen Daten. Sofern Sie sich registrieren, verweisen wir Sie auf den Abschnitt "Registrierung auf unserer Webseite" innerhalb unserer Datenschutzerklärung.
Auflösung von Hämatit
Moderator: Chemiestudent.de Team
-
Jörg24
- Laborratte

- Beiträge: 5
- Registriert: 25.04. 2013 17:36
- Hochschule: keine angeführte Hochschule
Auflösung von Hämatit
Hallo,
Ich habe da noch ein Beispiel bei dem ich nicht einmal ansatzweise weis wie ich hier beginnen soll.
T=298°K
Gegen sind: delta r H^0 (10^5 J mol^-1) delta r S^0 (J mol^-1 K^-1)
Fe2=3(s) -8,24 87,4
Fe^3+ (aq) -0,485 -315,9
H^+ (aq) 0 0
H2O (l) -2,86 69,91
a) Die Auflösungsreaktion von Hämatit in Wasser und die zugehörige "mass law equation".
b) Löslichkeitsprodukt berechnen
c) Fe^3+ Aktivität bei pH=8 berechnen
Ich habe Punkt a Teilweise zusammengebracht, aber da stimmt was mit den Ladungen leider nicht. Und ich weis leider überhaupt nicht wie ich die Angaben richtig einsetze.
Ich hoffe es kann mir hier jemand zeigen,
Danke!
Ich habe da noch ein Beispiel bei dem ich nicht einmal ansatzweise weis wie ich hier beginnen soll.
T=298°K
Gegen sind: delta r H^0 (10^5 J mol^-1) delta r S^0 (J mol^-1 K^-1)
Fe2=3(s) -8,24 87,4
Fe^3+ (aq) -0,485 -315,9
H^+ (aq) 0 0
H2O (l) -2,86 69,91
a) Die Auflösungsreaktion von Hämatit in Wasser und die zugehörige "mass law equation".
b) Löslichkeitsprodukt berechnen
c) Fe^3+ Aktivität bei pH=8 berechnen
Ich habe Punkt a Teilweise zusammengebracht, aber da stimmt was mit den Ladungen leider nicht. Und ich weis leider überhaupt nicht wie ich die Angaben richtig einsetze.
Ich hoffe es kann mir hier jemand zeigen,
Danke!
-
Auwi
- Rührfischangler

- Beiträge: 67
- Registriert: 21.03. 2013 09:25
- Hochschule: Bonn: Rheinische Friedrich-Wilhelms-Universität
Re: Auflösung von Hämatit
Hämatit ist Fe2O3
Die "Auflösung" erfolgt in Wasser also nach der Gleichung:
Fe2O3 (s) + 3 H2O (l) -> 2 Fe 3+ (aq) + 6 OH - (aq)
Jetzt rechnest Du gemäß Summe(Produkte) - Summe(Edukte)
über die einzelnen H-T*S Werte die freie Reaktionsenthalpie G aus, mit der Du dann
mittels G = -RT*ln(K)
die Gleichgewichtskonstante K berechnen kannst.
Aus der kannst Du dann die Aktivitäten berechnen.
Wenn Du dann G oder K berechnet hast, helfe ich Dir gern bei der Berechnung der gesuchten Aktivität weiter !
Mir ist es in diesem Forum zu mühsam Herleitungen und Rechnungen darzustellen
Die "Auflösung" erfolgt in Wasser also nach der Gleichung:
Fe2O3 (s) + 3 H2O (l) -> 2 Fe 3+ (aq) + 6 OH - (aq)
Jetzt rechnest Du gemäß Summe(Produkte) - Summe(Edukte)
über die einzelnen H-T*S Werte die freie Reaktionsenthalpie G aus, mit der Du dann
mittels G = -RT*ln(K)
die Gleichgewichtskonstante K berechnen kannst.
Aus der kannst Du dann die Aktivitäten berechnen.
Wenn Du dann G oder K berechnet hast, helfe ich Dir gern bei der Berechnung der gesuchten Aktivität weiter !
Mir ist es in diesem Forum zu mühsam Herleitungen und Rechnungen darzustellen
-
Jörg24
- Laborratte

- Beiträge: 5
- Registriert: 25.04. 2013 17:36
- Hochschule: keine angeführte Hochschule
Re: Auflösung von Hämatit
Danke!!!
Bei G bekomme ich diese Werte raus:
G Hämatit=(8,24*10^5)-298*87,4=-850045,2
G Fe^3+ =45638,2
G H+=0
G H2O =-306833,18
G gesamt= Produkte-Edukte= 2*G von Fe -3* G von H2O -G von Fe2O3= 1861821,14
K=e^(-G/(R*T))= kein sinnvolles Ergebnis bei dem G wert.
Was hab ich da falsch gemacht?
Dieser Wert erscheint mir aber merkwürdig.
Bei G bekomme ich diese Werte raus:
G Hämatit=(8,24*10^5)-298*87,4=-850045,2
G Fe^3+ =45638,2
G H+=0
G H2O =-306833,18
G gesamt= Produkte-Edukte= 2*G von Fe -3* G von H2O -G von Fe2O3= 1861821,14
K=e^(-G/(R*T))= kein sinnvolles Ergebnis bei dem G wert.
Was hab ich da falsch gemacht?
Dieser Wert erscheint mir aber merkwürdig.
-
Auwi
- Rührfischangler

- Beiträge: 67
- Registriert: 21.03. 2013 09:25
- Hochschule: Bonn: Rheinische Friedrich-Wilhelms-Universität
Re: Auflösung von Hämatit
Ich habe mal die Freien Bildungsenthalpien aus der folgenden Tabelle entnommen:
http://www.chempage.de/Tab/thermo.htm
Hämatit: -742,2 kJ/mol
Fe(3+)aq = -481,2 kJ/mol
OH(-) aq = -229,99 kJ/mol
H2O = -237,13 kJ/mol
Das ergab bezüglich der von mir angegebenen Reaktionsgleichung:
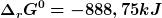
unhd damit ein
OK, da kann was nicht stimmen an dem "Lösungsweg".
Ich denke nochmal drüber nach
http://www.chempage.de/Tab/thermo.htm
Hämatit: -742,2 kJ/mol
Fe(3+)aq = -481,2 kJ/mol
OH(-) aq = -229,99 kJ/mol
H2O = -237,13 kJ/mol
Das ergab bezüglich der von mir angegebenen Reaktionsgleichung:
unhd damit ein
OK, da kann was nicht stimmen an dem "Lösungsweg".
Ich denke nochmal drüber nach
-
Auwi
- Rührfischangler

- Beiträge: 67
- Registriert: 21.03. 2013 09:25
- Hochschule: Bonn: Rheinische Friedrich-Wilhelms-Universität
Re: Auflösung von Hämatit
Über Google habe ich gefunden, daß das Löslichkeitsprodukt von Hämatit bei
 liegen soll.
liegen soll.
-
Jörg24
- Laborratte

- Beiträge: 5
- Registriert: 25.04. 2013 17:36
- Hochschule: keine angeführte Hochschule
Re: Auflösung von Hämatit
Ok, Danke!
Aber diese Werte erscheinen mir als extrem.
Aber das ist ja richtig, oder:
[delta r H^0 (J mol^-1)]-298*[delta r S^0 (J mol^-1 K^-1)]=delta G°
delta G°=delta H°-T* delta S°
deltaG°/(-RT)=ln(K)
ln(K)=deltaG°/(-8,3145*298)
Ich hab dann das [ln(K) von 2 mal Fe2+] minus [ln(K) von Fe2O3+ ln(K) von 3 mal H2O] genommen. Also ln(k) der Produkte- ln(k) der Edukte
Da bekomme ich jetzt als wert -751,45 raus.
Aber diese Werte erscheinen mir als extrem.
Aber das ist ja richtig, oder:
[delta r H^0 (J mol^-1)]-298*[delta r S^0 (J mol^-1 K^-1)]=delta G°
delta G°=delta H°-T* delta S°
deltaG°/(-RT)=ln(K)
ln(K)=deltaG°/(-8,3145*298)
Ich hab dann das [ln(K) von 2 mal Fe2+] minus [ln(K) von Fe2O3+ ln(K) von 3 mal H2O] genommen. Also ln(k) der Produkte- ln(k) der Edukte
Da bekomme ich jetzt als wert -751,45 raus.
-
Auwi
- Rührfischangler

- Beiträge: 67
- Registriert: 21.03. 2013 09:25
- Hochschule: Bonn: Rheinische Friedrich-Wilhelms-Universität
Re: Auflösung von Hämatit
Hast Du Dir mal überlegt, welche Reaktion Du dieser "Berechnung" zugrunde gelegt hast?Ich hab dann das [ln(K) von 2 mal Fe2+] minus [ln(K) von Fe2O3+ ln(K) von 3 mal H2O] genommen. Also ln(k) der Produkte- ln(k) der Edukte
Das kann doch so nicht funktionieren ...
-
kaka
- Assi-Schreck

- Beiträge: 246
- Registriert: 26.10. 2012 13:10
- Hochschule: keine angeführte Hochschule
Re: Auflösung von Hämatit
Ergebnis meiner Suche :Auwi hat geschrieben:Ich habe mal die Freien Bildungsenthalpien aus der folgenden Tabelle entnommen:
Fe(3+)aq = -481,2 kJ/mol
OH(-) aq = -229,99 kJ/mol
Fe(3+)aq : - 4,7 kJ/mol
OH(-)aq : - 157,2 kJ/mol
Friedrich Karl Schmidt
www.treffpunkt-naturwissenschaft.com
www.treffpunkt-naturwissenschaft.com
Wer ist online?
Mitglieder in diesem Forum: 0 Mitglieder und 2 Gäste