kationische polymerisation
Verfasst: 03.10. 2007 17:52
Hallo,
ich habe eine Frage zur kationischen Polymerisation.
Wie es zu der Bildung dieses Koplexes kommt ist mir klar. Es liegt daran, dass AlCl2 eine Elektronenmangelverbindung ist. Das Wasser stellt also seine Elektronen bereit und splatet danach ein Wasserstoffproton ab. Fungiert also als Protonendonator nach Brönstedt.
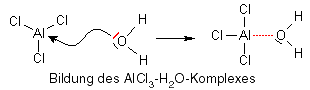
Jetzt aber zu meiner Frage:
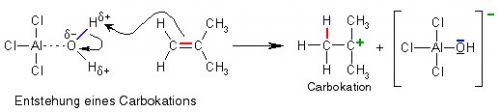
Warum reagiert das H+ Proton mit der Doppelbindung. Ist dies nun ein energetisch günstigerer Zustand und wenn ja warum?
ich habe eine Frage zur kationischen Polymerisation.
Wie es zu der Bildung dieses Koplexes kommt ist mir klar. Es liegt daran, dass AlCl2 eine Elektronenmangelverbindung ist. Das Wasser stellt also seine Elektronen bereit und splatet danach ein Wasserstoffproton ab. Fungiert also als Protonendonator nach Brönstedt.

Jetzt aber zu meiner Frage:

Warum reagiert das H+ Proton mit der Doppelbindung. Ist dies nun ein energetisch günstigerer Zustand und wenn ja warum?