Peptide (Schutzgruppen)
Nach der Reaktion muß die Schutzgruppe wieder entfernt werden. Die aktivierende Gruppe an der Säurefunktion wird durch eine andere Aminosäure ersetzt und somit bei der Reaktion schon abgespalten.
- Aminogruppe:
Die Schutzgruppe bewirken, daß der Stickstoff "nicht mehr" nucleophil ist. Da die Aminosäure als Zwitterion vorliegt, muß man Base zugeben, damit kein Amoniumion vorliegt.
Man verwendet zum Beispiel:- tert.-Butyloxycarbonyl-Methode:
Als Schutzgruppe führt man den sogennanten BOC-Rest ein. Dieser wird nach der Reaktion leicht mit CF3COOH abgespalten.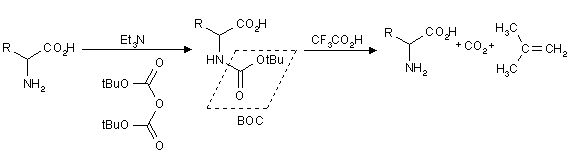
- Benzyloxycarbonyl-Methode:
Hier benutzt man als Schutzgruppe am Stickstoff den Benzylcarbonyl-Rest (früher Carbobenzoxy-Rest; kurz Cbz- oder Z-Rest).Die Gruppe wird nach der Reaktion durch katalytische Hydrierung abgespalten.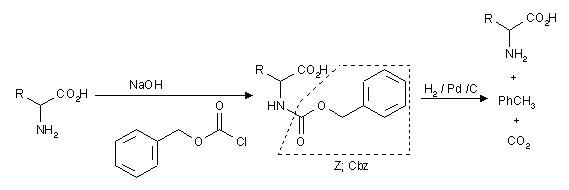
- tert.-Butyloxycarbonyl-Methode:
- Säuregruppe:
Die Säurefunktion wird durch geeignete Gruppen aktiviert. Man verwendet zum Beispiel die Chloride oder Azide.
Schonend kann man mit folgenden Gruppen aktivieren:- Isobutyloxycarbonyl-Methode:
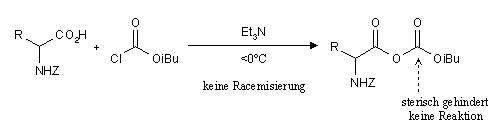
- Carbodiimid-Methode:
Als aktivierende Gruppe verwendet man DCC (=Dicyclohexylcarbodiimid).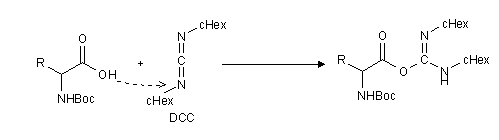
- Isobutyloxycarbonyl-Methode:
- Erlenmeyer-Synthese
- Streckersynthese
| Zusätzlich zu der hier online verfügbaren Namensreaktionen könnt Ihr auch die ganze Liste als PDF herunterladen. |
Mit freundlicher Genehmigung von Andreas Schleifenbaum und Thomas Wohlhaupter
